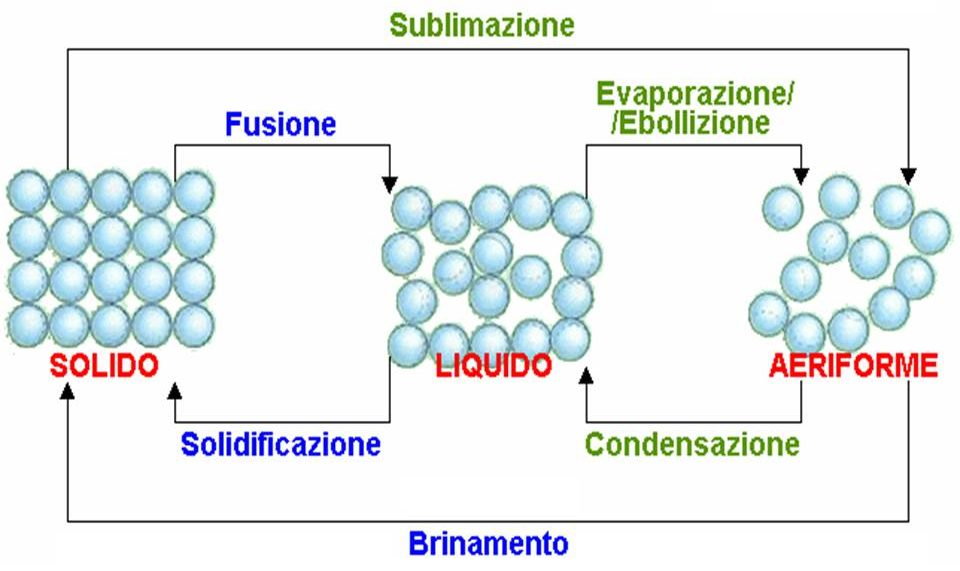
Sulla Terra la materia si presenta in tre forme diverse: stato solido, stato liquido e stato gassoso (o aeriforme). Mediante scambi di calore si può ottenere il passaggio da uno stato di aggregazione all’altro.
Le particelle che formano la materia sono soggette a due tipi di azioni contrastanti: le forze di attrazione, ovvero le FORZE DI COESIONE, che tendono a farle restare unite, e l’agitazione termica che, invece, tende a farle staccare. Il prevalere dell’una o dell’altra determina il loro stato di aggregazione. poiché le forze di coesione dipendono dalle caratteristiche di ogni sostanza, è la variazione di temperatura che influenza il passaggio da uno stato all’altro. Al crescere della temperatura, infatti, cresce l’agitazione termica, i legami si indeboliscono e si passa dallo stato solido a quello liquido. Se si fornisce ancora calore l’agitazione termica aumenta e si spezzano anche quei tenui legami presenti nello stato liquido, si passa così allo stato gassoso.
Sottraendo calore, al contrario, l’agitazione termica diminuisce e tornano a prevalere le forze di coesione tra le particelle. Si passa così dallo stato gassoso a quello liquido e , se il raffreddamento continua, a quello solido.

PASSAGGIO SOLIDO – LIQUIDO
Se forniamo calore a un oggetto solido, questo dapprima si riscalda. A un certo punto, però, accade qualcosa di diverso: l’oggetto inizia a diventare liquido.
È questo il fenomeno della fusione.
La fusione di un solido segue tre leggi sperimentali:
- a una data pressione, per ogni sostanza la fusione avviene a una temperatura determinata, detta temperatura di fusione di quella sostanza;
- durante tutto l’intervallo di tempo in cui avviene la fusione di un corpo, la sua temperatura si mantiene costante;
- l’energia necessaria per fondere completamente una massa m di una data sostanza, che si trova
In un solido le particelle sono disposte in modo ordinato in posizioni ben definite. In seguito a riscaldamento si raggiunge la TEMPERATURA DI FUSIONE e si ha il passaggio dallo stato solido allo stato liquido cioè la FUSIONE.
Il passaggio da liquido a solido si chiama SOLIDIFICAZIONE e si ottiene raffreddando la sostanza fino ad una T inferiore alla sua T di fusione.

A. Dapprima la temperatura dello stagno solido aumenta in modo proporzionale agli intervalli di tempo trascorsi;
B. per tutta la durata del processo di fusione, la temperatura dello stagno si mantiene costante a 232 °C;
C. quando tutto lo stagno è divenuto liquido, la sua temperatura ricomincia a salire.
PASSAGGIO LIQUIDO – GAS
In un liquido le particelle sono disposte in modo disordinato e sono abbastanza libere di muoversi. Quelle presenti nella sua parte superficiale tendono a passare allo stato di vapore a qualsiasi temperatura. Questo fenomeno prende il nome di EVAPORAZIONE.
Quando in seguito al riscaldamento, si raggiunge la Temperatura di ebollizione anche le particelle presenti nella parte interna del liquido passano allo stato vapore.
Anche per l’ebollizione di un liquido si ricavano tre leggi sperimentali:
- a una data pressione, per ogni liquido l’ebollizione avviene a una temperatura determinata, detta temperatura di ebollizione;
- durante tutto l’intervallo di tempo in cui avviene l’ebollizione di un liquido, la sua temperatura si mantiene costante;
- l’energia necessaria per trasformare in vapore l’intera massa m di un liquido, che si trova già alla temperatura di ebollizione, è direttamente proporzionale a m.
La terza legge è espressa dalla formula

La costante Lv è detta calore latente di vaporizzazione e si misura in joule/ kilogrammo. È numericamente uguale alla quantità di energia necessaria per trasformare completamente in vapore 1 kg di una data sostanza. Se l’energia fornita è sotto forma di calore la formula precedente si scrive così
Q = Lv m.
PASSAGGIO SOLIDO – GAS
Il passaggio da solido a gas è detto SUBLIMAZIONE ed avviene direttamente senza passare attraverso la fase liquida. (Es: NAFTALINA).
Il passaggio inverso si chiama BRINAMENTO.
TRATTO AB
Riscaldando un solido aumenta l’agitazione termica delle particelle e la temperatura aumenta.
Quando l’energia delle oscillazioni supera l’energia di legame tra le particelle del solido ha inizio la FUSIONE.
TRATTO BC
Il calore fornito durante la fusione viene impiegato per rompere i legami, la temperatura si mantiene costante al valore della T di fusione fino alla completa fusione del solido.
CALORE LATENTE DI FUSIONE Calore che non produce riscaldamento della sostanza ma ne permette il passaggio di stato fisico.
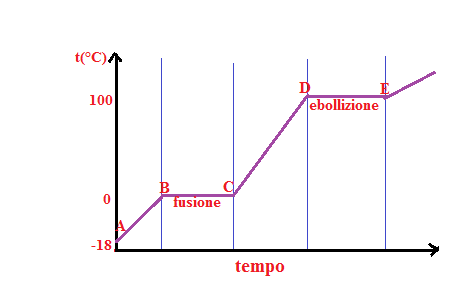
TRATTO CD
Quando tutta la massa è passata allo stato liquido, continuando a fornire calore si osserverà di nuovo un incremento di T proporzionale alla quantità di calore fornita. Al crescere di T, aumenta il numero di particelle di liquido dotate di energia sufficiente a passare in fase vapore e si ha evaporazione lenta e continua.
TRATTO DE
Quando la T raggiunge un valore tale che la pressione di vapore raggiunge la pressione esterna si ha l’ebollizione, la t ora si mantiene costante finché tutto il liquido sarà evaporato → CALORE LATENTE DI EVAPORAZIONE: produce il passaggio di stato senza produrre riscaldamento. A quel punto la T ricomincerà a salire e si avrà il riscaldamento della fase vapore.
La terza legge della fusione è espressa mediante la formula

La costante Lf è detta calore latente di fusione e si misura in joule/kilogrammo.
È numericamente uguale alla quantità di energia necessaria per fondere completamente 1 kg di una data sostanza. Per esempio, per fondere 1 kg di ghiaccio, che si trova già alla temperatura di 0 °C, occorre fornire 334 kJ di energia.
Di solito forniamo al ghiaccio questa energia mediante scambi di calore e in questo caso la formula precedente diventa Q = Lf m, ma potremmo fornirla anche mediante un lavoro meccanico di spezzettamento.