L’equilibrio di autoionizzazione dell’acqua, che si verifica quando si sciolgono in essa uno o più soluti, è il seguente:
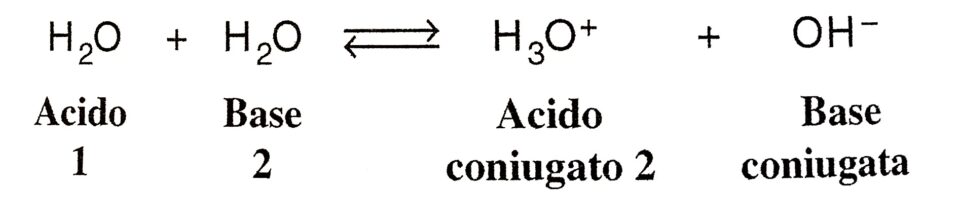
Il comportamento dell’acqua è anfotero poiché alcune molecole cedono un protone comportandosi da acido mentre altre lo accettano comportandosi da base.
Per l’equilibrio di auto ionizzazione dell’acqua, come per tutte le reazioni di equilibrio ionico, si può scrivere la seguente espressione:

La concentrazione di H2O viene assunta costante e viene inglobata nella costante di equilibrio K. Si ricava così il prodotto ionico dell’acqua KW, che, alla temperatura di 25 °C, vale 1,0 × 10-14.
KW = [H3O+] [OH–] = 1,0 x 10-14
KW aumenta con la temperatura perché il processo di autoionizzazione è endotermico (ΔH>0).
In acqua pura [H3O+] è uguale a [OH–] e cioè:

Per evitare di usare una notazione esponenziale per si ricorre all’operatore p che corrisponde all’opposto del logaritmo decimale (-log):
pH = -log [H3O+] e pOH = -log [OH–]
Dal prodotto ionico, usando i logaritmi, si ricava:
pKw = pH + pOH = 14 pH = pKw – pOH e pOH = pKw – pH
Una soluzione si definisce neutra quando:
[H3O+] = [OH–] = 10-7 M
e quindi quando:
pH = pOH = 7
Si definisce:
- acida quando pH <7 (ed il valore di pOH > 7),
- alcalina o basica quando pH > 7 (pOH < 7).